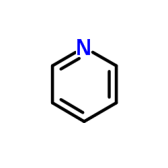
[ 密度 ]:1.0±0.1 g/cm³
[ 沸点 ]:115.3±0.0 ℃ at 760 mmHg
[ 熔点 ]:-42 ℃
[ 分子式 ]:C5H5N
[ 分子量 ]:79.100
[ 闪点 ]:20.0±0.0 ℃
[ 精确质量 ]:79.042198
[ PSA ]:12.89000
[ LogP ]:0.73
[ 外观性状 ]:透明干净的液体带有特有的气味
[ 蒸汽密度 ]:2.72 (vs air)
[ 蒸汽压 ]:22.8±0.2 mmHg at 25℃
[ 折射率 ]:1.501
[ 储存条件 ]:
1.储存于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃。
2.应与氧化剂、酸类、食用化学品分开存放,切忌混储。采用防爆型照明、通风设施。
3.禁止使用易产生火花的机械设备和工具。
4.储区应备有泄漏应急处理设备和合适的收容材料。
[ 稳定性 ]:
1.常温常压不分解。禁止与酸类、强氧化剂、氯仿接触。不宜使用铜制容器。贮存时避免和强氧化剂如过氧化物、硝酸等放在一起。
化学性质有弱碱性(Kb 2.3× 10-9,pKa5.17),碱性比哌啶(Kb 1.6× 10-3)弱,但比苯胺(Kb3.8× 10-10)稍强。吡啶除与盐酸、氢溴酸、苦味酸等生成盐外,与三氟化硼也能组成化合物。与锌、汞、钴、镍等金属盐类组成加成化合物。与卤代烷作用生成季铵盐。在金属催化剂存在下易被氢还原成哌啶。若用电解还原也主要生成哌啶,用氢化铝锂还原生成二氢吡啶,用氢化硼钠还原生成四氢吡啶。
2.吡啶对氧化剂比较稳定,不被硝酸、氧化铬、高锰酸钾等所氧化,故在用高锰酸盐进行的氧化反应中可作溶剂使用。对过氧化氢或过酸作用变成N-氧化物(C5H5NO)。
3.吡啶很难发生亲电取代反应,也不发生Friedel Crafts反应。硝化时需要300℃的高温才能得到3-硝基吡啶,且收率低。但容易发生亲核取代反应。例如与氨基钠作用生成2-氨基吡啶。用铂或碱作催化剂与重水作用时,吡啶第二位的氢可与重氢发生交换。
[ 水溶解性 ]:Miscible
[ 凝固点 ]:-42℃
[ 分子结构 ]:
1、 摩尔折射率:24.34
2、 摩尔体积(cm³/mol):82.6
3、 等张比容(90.2K):201.4
4、 表面张力(dyne/cm):35.2
5、 极化率(10⁻²⁴cm³):9.65
[ 计算化学 ]:
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:1
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积12.9
7.重原子数量:6
8.表面电荷:0
9.复杂度:30.9
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
[ 更多 ]:
1. 性状:无色液体,具有特殊的臭味。
2. 沸点(℃,101.3kPa):115.32-115.3
3. 熔点(℃):-41.6
4. 相对密度(g/mL,20/4℃):0.9831
5. 相对密度(g/mL,25/4℃):0.9780
6. 相对蒸汽密度(g/mL,空气=1):2.73
7. 折射率(20℃):1.51016
8. 折射率(25℃):1.5073
9. 黏度(mPa· s,15℃):1.038
10. 黏度(mPa· s,20℃):0.952
11. 黏度(mPa· s,30℃):0.829
12. 闪点(℃,闭口):20
13. 燃点(℃):482
14. 蒸发热(KJ/mol,25℃):40.4277
15. 熔化热(KJ/mol):7.4133
16. 生成热(KJ/mol,液体):99.9808
17. 燃烧热(KJ/mol,定压):2826.51
18. 燃烧热(KJ/mol,定容):2782.97
19. 比热容(KJ/(kg· K) ,21℃,定压):1.64
20. 临界温度(℃):346.85
21. 临界压力(MPa):6.18
22. 沸点上升常数:2.69
23. 电导率(S/m,25℃):4.0× 10-8
24. 热导率(W/(m· K),20℃):0.182
25. 蒸气压(kPa,25℃):2.67
26. 爆炸下限(%,V/V):1.8
27. 爆炸上限(%,V/V):12.4
28. 体膨胀系数(K-1,0~90℃):0.001122
29. 溶解性:能与水、醇、醚、石油醚、苯、油类等多种溶剂混溶。能溶解多种有机化合物与无机化合物。